Azotek boru
| |||||||||||||||||||||||||||||||||||||||||||||||
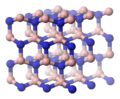 układ wurcytu | |||||||||||||||||||||||||||||||||||||||||||||||
| Ogólne informacje | |||||||||||||||||||||||||||||||||||||||||||||||
| Wzór sumaryczny |
BN | ||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Masa molowa |
24,82 g/mol | ||||||||||||||||||||||||||||||||||||||||||||||
| Identyfikacja | |||||||||||||||||||||||||||||||||||||||||||||||
| Numer CAS | |||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | |||||||||||||||||||||||||||||||||||||||||||||||
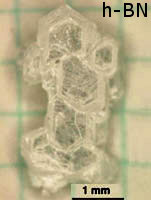
Azotek boru, BN – nieorganiczny związek chemiczny boru i azotu. Po raz pierwszy został otrzymany w 1842 roku. Podobnie jak diament, azotek boru może zostać wytworzony w taki sposób, aby miał własności półprzewodnikowe.
W zależności od ciśnienia i temperatury azotek boru może występować w trzech strukturach krystalicznych: heksagonalnej (hBN), regularnej (cBN) i wurtzytowej (wBN)[3]:
- Azotek boru heksagonalny (hBN, α-BN), znany również jako "biały grafit", ma strukturę warstwową, jest izolatorem elektrycznym i charakteryzuje się wysoką przewodnością cieplną.
- Zastosowania: lubrykanty wysokotemperaturowe, materiały do rozpraszania ciepła w urządzeniach elektronicznych, elementy izolacyjne w piecach próżniowych.
- Azotek boru regularny (borazon, elbor, cBN, c-BN, β-BN) ma strukturę podobną do diamentu; cechuje się dużą twardością oraz stabilnością termiczną i chemiczną[3]. Został wytworzony po raz pierwszy w 1957 roku przez R.H. Wentorfa w USA, za pomocą aparatury stosowanej do uzyskiwania syntetycznych diamentów[4]. Twardość kryształów borazonu oceniana jest na 90 do 95% twardości diamentów, charakteryzuje się on jednak większą odpornością chemiczną i może być stosowany do obróbki żelaza. Ma też znacznie większą odporność termiczną. Jego największą wadą jest cena – średnio o 30% wyższa niż diamentu[potrzebny przypis].
- Zastosowania: materiały ścierne, narzędzia skrawające, elementy do pracy w ekstremalnych warunkach temperaturowych i środowiskowych[3]. Wykorzystywany jest zwłaszcza do obróbki ściernej o wysokich prędkościach, np. do szlifowania i cięcia stali hartowanych. W przeciwieństwie do narzędzi diamentowych nie rozkłada się pod wpływem temperatury (powinowactwo chemiczne węgla – pod każdą postacią, diamentu też – do żelaza w stali). Borazon jest co prawda bardziej miękki od diamentu (5000 HV30 – borazon, 8000–10000 HV30 – diament), ale nie traci mocno na twardości podczas ogrzewania (do ok. 1500 °C), dlatego jest używany do szlifowania węglików i diamentów w wysokich temperaturach[potrzebny przypis].
- Azotek boru wurtzytowy (wBN) to bardzo rzadka forma, powstająca pod wysokim ciśnieniem; może być twardszy niż diament.
- Potencjalne zastosowania: badania materiałów o najwyższej twardości, aplikacje wysokociśnieniowe, powłoki ochronne o wysokiej wydajności.
Otrzymywanie
Do otrzymywania azotku boru używa się tlenku boru(III) i azotu atmosferycznego. Reakcja zachodzi w wysokich temperaturach i wymaga obecności Ca
3(PO
4)
2 jako katalizatora. Zamiast azotu może zostać użyty amoniak. Powstaje przy tym bezbarwna forma heksagonalna (alfa), o strukturze analogicznej do struktury grafitu i podobnych własnościach fizycznych. Można z niej uzyskać formę beta (borazon), przez ogrzanie do ok. 1750 °C, przy ciśnieniu 70 kbar i obecności azotku litu.
Przypisy
- ↑ a b c Boron nitride (nr 255475) – karta charakterystyki produktu Sigma-Aldrich (Merck) na obszar Polski. [dostęp 2012-02-07]. (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ Azotek boru (nr 255475) (ang.) – karta charakterystyki produktu Sigma-Aldrich (Merck) na obszar Stanów Zjednoczonych. [dostęp 2012-02-07]. (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ a b c Boron Nitride, BN Ceramic Materials - Structures & Applications [online], sekcja „Introduction”, Stanford Advanced Materials [dostęp 2025-09-18] (ang.).
- ↑ R.H. Wentorf, Cubic Form of Boron Nitride, „The Journal of Chemical Physics”, 26 (4), 1957, s. 956–956, DOI: 10.1063/1.1745964 [dostęp 2025-09-18] (ang.).


